Brain clocks capture diversity and disparities in aging and dementia across geographically diverse populations
Moguilner, S., Baez, S., Hernández, H. […] García, A. M. […] & Ibáñez A (2024). Brain clocks capture diversity and disparity in aging and dementia. Nature Medicine.
Los relojes cerebrales, que cuantifican las discrepancias entre la edad cerebral y la cronológica, son prometedores para comprender la salud y las enfermedades cerebrales. Sin embargo, se desconoce el impacto de la diversidad (geográfica, socioeconómica, sociodemográfica, de sexo y de neurodegeneración) en la brecha entre la edad cerebral y la cronológica. Analizamos conjuntos de datos de 5.306 participantes de 15 países (7 países de América Latina y el Caribe (ALC) y 8 países no ALC). Basándonos en interacciones de orden superior, desarrollamos una arquitectura de aprendizaje profundo de la brecha de edad cerebral para imágenes de resonancia magnética funcional (2.953) y electroencefalografía (2.353). Los conjuntos de datos comprendían controles sanos e individuos con deterioro cognitivo leve, enfermedad de Alzheimer y demencia frontotemporal variante conductual. Los modelos LAC mostraron edades cerebrales más avanzadas (resonancia magnética funcional: error direccional medio = 5,60; error cuadrático medio [e.c.m.r.] = 11,91; electroencefalografía: error direccional medio = 5,34; e.c.m.r. = 9,82) asociadas a redes fronto-posteriores en comparación con los modelos no LAC. La desigualdad socioeconómica estructural, la contaminación y las disparidades sanitarias fueron predictores influyentes del aumento de las brechas cerebro-edad, especialmente en ALC (R² = 0,37, F² = 0,59, r.m.s.e. = 6,9). Se observó una brecha de edad cerebral ascendente desde los controles sanos hasta el deterioro cognitivo leve y la enfermedad de Alzheimer. En LAC, se observaron mayores brechas de edad cerebral en las mujeres de los grupos de control y enfermedad de Alzheimer en comparación con los respectivos varones. Los resultados no se explicaron por variaciones en la calidad de la señal, demografía o métodos de adquisición. Estos hallazgos proporcionan un marco cuantitativo que capta la diversidad del envejecimiento cerebral acelerado.
Para acceder al artículo, hacé click aquí.
Brain clocks capture diversity and disparities in aging and dementia across geographically diverse populations
Moguilner, S., Baez, S., Hernández, H. […] García, A. M. […] & Ibáñez A (2024). Brain clocks capture diversity and disparity in aging and dementia. Nature Medicine.
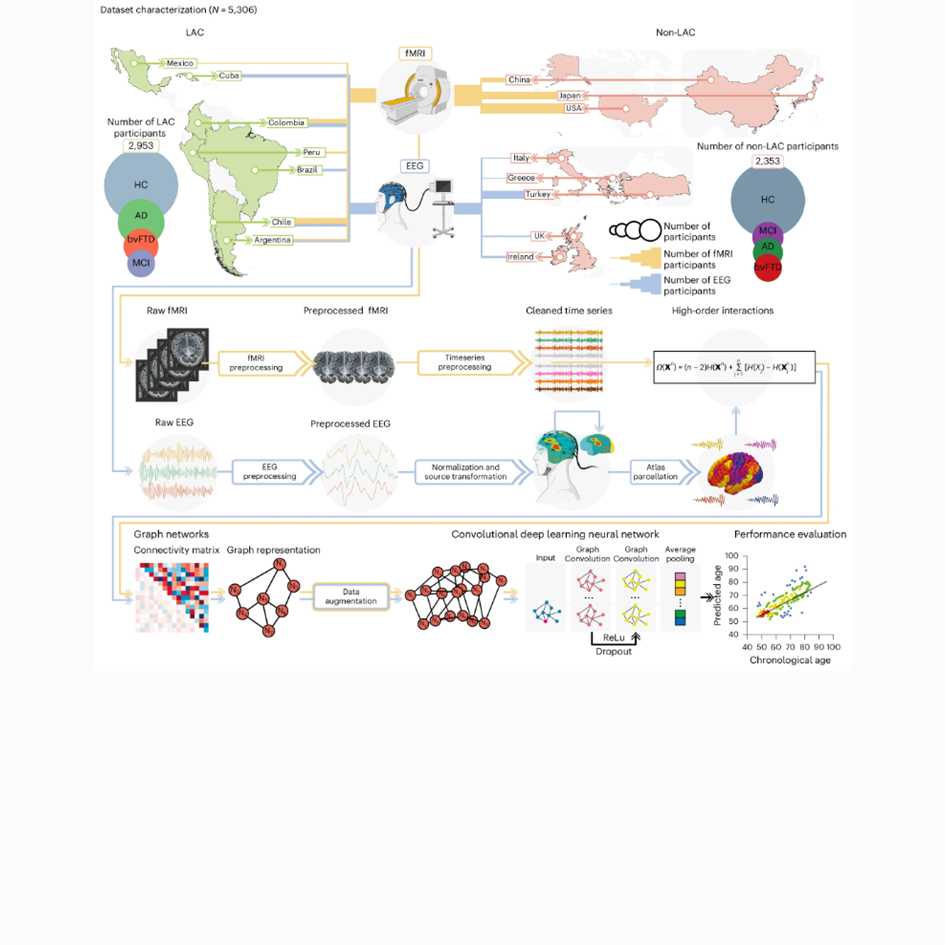
Brain clocks, which quantify discrepancies between brain age and chronological age, hold promise for understanding brain health and disease. However, the impact of diversity (including geographical, socioeconomic, sociodemographic, sex and neurodegeneration) on the brain-age gap is unknown. We analyzed datasets from 5,306 participants across 15 countries (7 Latin American and Caribbean countries (LAC) and 8 non-LAC countries). Based on higher-order interactions, we developed a brain-age gap deep learning architecture for functional magnetic resonance imaging (2,953) and electroencephalography (2,353). The datasets comprised healthy controls and individuals with mild cognitive impairment, Alzheimer disease and behavioral variant frontotemporal dementia. LAC models evidenced older brain ages (functional magnetic resonance imaging: mean directional error = 5.60, root mean square error (r.m.s.e.) = 11.91; electroencephalography: mean directional error = 5.34, r.m.s.e. = 9.82) associated with frontoposterior networks compared with non-LAC models. Structural socioeconomic inequality, pollution and health disparities were influential predictors of increased brain-age gaps, especially in LAC (R² = 0.37, F² = 0.59, r.m.s.e. = 6.9). An ascending brain-age gap from healthy controls to mild cognitive impairment to Alzheimer disease was found. In LAC, we observed larger brain-age gaps in females in control and Alzheimer disease groups compared with the respective males. The results were not explained by variations in signal quality, demographics or acquisition methods. These findings provide a quantitative framework capturing the diversity of accelerated brain aging.
To access the full paper, please click here.